研发体系介绍
源头创新药物的研发,涉及多学科的交叉融合。微芯生物核心研发管理团队由留美及国内长期从事药物研发和管理的专业人士组成,具有丰富的国际制药/生物技术企业管理、研发经验,熟知全球药品管理技术法规和专利策略。研发团队具有医学、药学、化学、生物学等专业/复合专业背景。高级研发人才团队具有靶点确认、探索性研究、分子模拟及设计、高通量高内涵筛选、生物标志物的转化医学研究等领域的专家知识,具备新药早期筛选评价、临床研究开发以及从实验室到商业化的研究、中试、质控及生产等核心能力。人才、技术、研发管理体系为公司原创新药研发提供了保障。
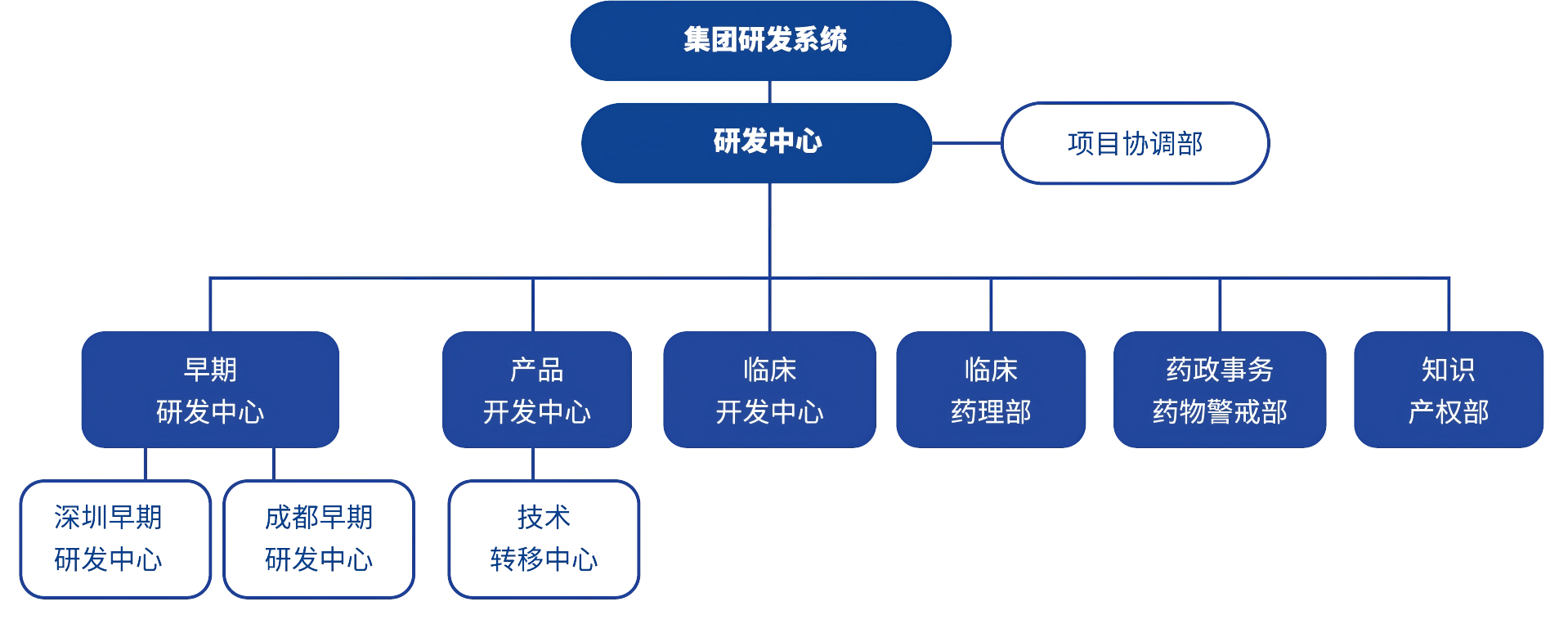
早期研发中心
微芯生物是中国原创新药领域的先行者。作为核心引擎的早期研发中心立足科学,坚持原创,始终关注临床未满足的治疗需求,持续开发具有显著临床差异化优势和市场潜力的创新药物。早期研发中心通过对深圳和成都早期研发中心的分领域统筹管理的模式,实现人力资源、研发资源的优化配置,加快产品研发及技术创新速度,给公司新产品的开发、上市提供有力保障。大分子早期研发中心(微芯新域)进一步丰富公司的创新药物形式和治疗手段。
临床开发中心
新机制、新适应症原创新药的临床开发策略和实践,显著区别于快速跟随新药和仿药。微芯生物在过去的二十余载里,探索和实践了符合原创新药临床开发规律的策略和模式,从早期临床试验到注册临床试验、从新药上市注册获批到上市后真实世界观察研究、从中国临床研究到国际临床开发,都具有成功案例,组建了一支全功能覆盖的临床开发团队,包括临床试验管理、医学、注册、运营、数据管理、统计、药代、药物安全等在内的成员分布于全国多个城市,保障了强有力的临床开发能力。
临床药理
通过临床药理学研究,全面了解创新药的人体药代和药效学特征,为临床开发方案制订提供科学依据,与早期研发中心、临床开发、产品开发、药政事务等团队共同推进创新药的药政审批和上市申请。
产品开发
产品开发是支持原创新药临床研究顺利开展和实现产业化的重要保障,保证了拟上市药物的质量可控性和安全性。随着原创新药研发进程的推进和对药物认知的逐渐深入,需结合临床研究、放大生产,不断完善药学研究工作,包括创新药工艺研究、杂质研究、质量研究,确保药品安全有效、质量可控,进一步保障在研产品的研发成功率。至今,微芯生物的产品开发系统通过西达本胺、西格列他钠与西奥罗尼三个原创新药项目,积累了丰富的实战经验与新产品开发的重要能力。
药政事务与药物警戒
负责临床试验申请、上市申报及药物安全信息收集上报。
知识产权
通过围绕产品开发以及生命周期管理相关的专利布局和专利维护,为公司创新药的市场价值和社会价值等核心利益提供法律保障。

